Вченим вдалося створити ефективну вакцину проти коронавірусу
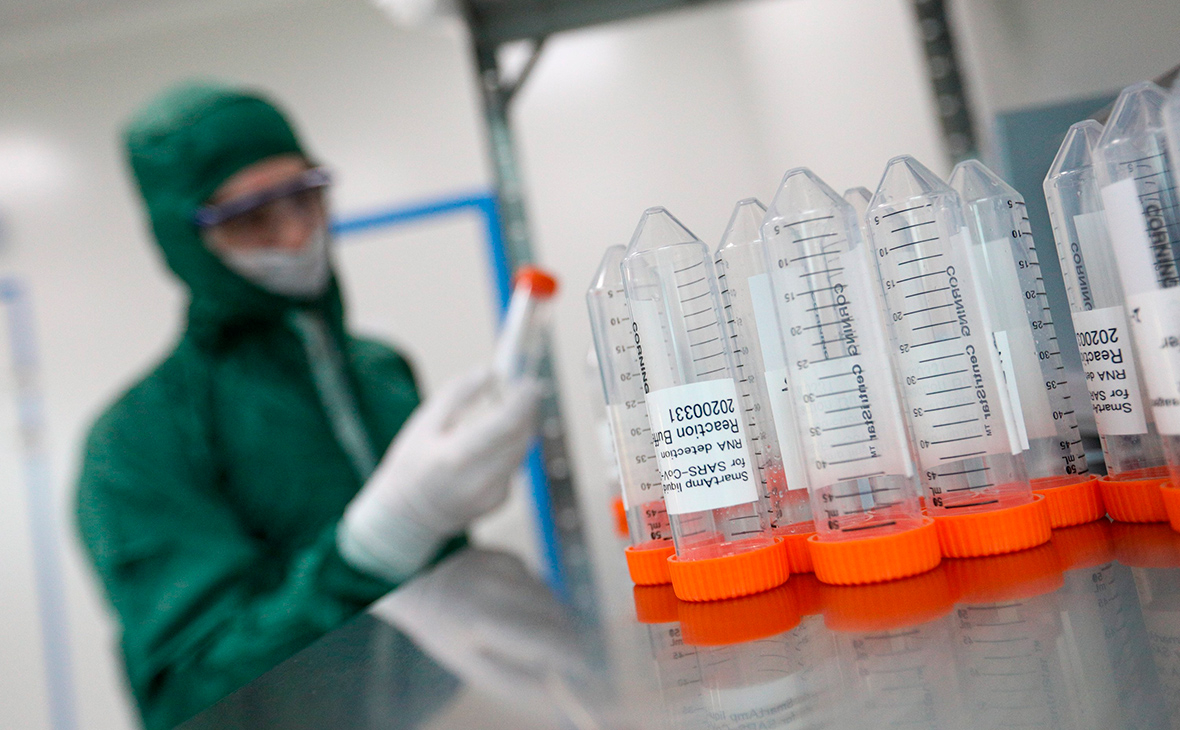
Експериментальна вакцина компанії Pfizer Inc PFE.N COVID-19 є більш ніж на 90% ефективною, про що свідчать результати первинних результатів випробувань, заявив у понеділок виробник ліків, – повідомляє “Reuters“.
Вчені, службовці охорони здоров’я та інвестори привітали перші успішні проміжні дані широкомасштабного клінічного випробування як переломний момент, який може допомогти перемогти пандемію, якщо успішними виявляться повні результати досліджень.
Однак масового впровадження, яке потребує схвалення законодавства, цього року не відбудеться. В той же час Pfizer та німецький партнер BioNTech SE 22UAy.F заявили, що поки не знайшли серйозних проблем з безпекою, і очікують, що цього місяця будуть вимагати дозволу на екстрене використання в США, підвищуючи шанс прийняти регуляторне рішення вже в грудні.
Якщо компанія отримає відповідну підтримку, цього року вона може випустити до 50 мільйонів доз, достатніх для захисту 25 мільйонів людей, а потім виробляти до 1,3 мільярда доз у 2021 році.
“Сьогодні чудовий день для науки та людства”, – сказав виконавчий директор Pfizer Альберт Бурла. Експерти заявили, що хочуть перевірити повні дані випробувань, але попередні результати виглядають обнадійливими.
«Ця новина змусила мене посміхнутися від вуха до вуха. Це полегшення – бачити такі позитивні результати щодо цієї вакцини», – сказав Пітер Горбі, професор з нових інфекційних захворювань в Оксфордському університеті.
Залишається ще багато питань, таких як ефективність вакцини за етнічним походженням чи віком та скільки може тривати такий імунітет. “Але підсумок полягає в тому, що як вакцина вона більш ніж на 90% ефективна, що надзвичайно“, – сказав вищий американський експерт з інфекційних хвороб доктор Ентоні Фаучі.
Компанія Pfizer розраховує отримати дозвіл на екстрене використання вакцини в США для людей у віці від 16 до 85 років. Для цього їй знадобляться два місяці подальших досліджень, щоб гарантувати відсутність побічних ефектів. Очікується, що це стане доступним у третьому тижні листопада. Міністр охорони здоров’я та соціальних служб США Алекс Азар заявив, що для отримання та обробки даних американськими регуляторами знадобиться кілька тижнів до їх потенційного затвердження.


